NộI Dung
- Sự khác biệt chính
- Biểu đồ so sánh
- Hợp chất ion là gì?
- Hợp chất phân tử là gì?
- Hợp chất ion so với hợp chất phân tử
Sự khác biệt chính
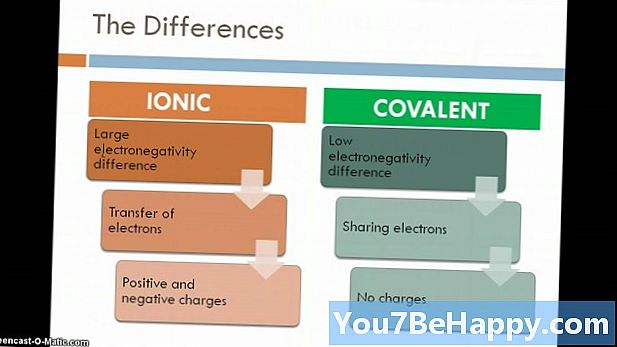
Hợp chất được công nhận là một chất được hình thành khi hai hoặc nhiều nguyên tố kết hợp với nhau theo tỷ lệ xác định thông qua một liên kết hóa học. Hợp chất ion là hợp chất được hình thành do lực hút tĩnh điện giữa kim loại và phi kim loại. Thông thường, các hợp chất ion xuất hiện ở trạng thái tinh thể bán. Hơn nữa, các hợp chất ion là chất dẫn điện tốt và có nhiệt độ nóng chảy và sôi cao. Mặt khác, Hợp chất phân tử được hình thành do sự chia sẻ các electron giữa hai phi kim loại. Liên quan đến hợp chất ion, chúng là chất dẫn điện kém và có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
Biểu đồ so sánh
| Hợp chất ion | Các hợp chất phân tử | |
| Sự hình thành | Các hợp chất ion được hình thành do lực hút tĩnh điện giữa kim loại và phi kim loại. | Các hợp chất phân tử được hình thành do sự chia sẻ các electron giữa hai phi kim. |
| Nhóm | Hợp chất ion được hình thành giữa kim loại và phi tinh thần. | Hợp chất phân tử được hình thành khi hai phi kim loại kết hợp hóa học |
| Liên kết | Hợp chất ion được hình thành do lực hút tĩnh điện được gọi là liên kết ion. | Các hợp chất phân tử được hình thành do liên kết cộng hóa trị giữa các nguyên tố. |
| Điểm nóng chảy và sôi | Cao | Thấp |
| Tiểu bang | Hợp chất ion luôn ở trạng thái rắn với sự hình thành tinh thể. | Hợp chất phân tử có thể ở bất kỳ trạng thái, rắn, lỏng hoặc khí ở nhiệt độ phòng. |
| Dây dẫn điện | Tốt | Xấu |
Hợp chất ion là gì?
Các hợp chất này được hình thành do lực hút tĩnh điện giữa kim loại và phi kim loại. Nói một cách đơn giản hơn, lực (liên kết ion) trong đó làm cho điện tích dương và điện tích âm phản ứng với nhau để tạo ra một hợp chất. Thông thường, các hợp chất ion xuất hiện ở trạng thái tinh thể được bán và là chất dẫn điện tốt với nhiệt độ nóng chảy và sôi cao. Hợp chất ion được hình thành giữa kim loại và phi kim loại, và có một số loại xuất hiện sáng bóng.
Thí dụ: Muối ăn (NaCl) là ví dụ phổ biến nhất của Hợp chất ion. Trong sự hình thành này, Natri (NA) là kim loại, trong khi Clo (Cl) là phi kim loại, cả hai đều được giữ với nhau do lực hút tĩnh điện giữa cả hai.
Hợp chất phân tử là gì?
Các hợp chất được hình thành do chia sẻ các electron giữa các phi kim loại được gọi là Hợp chất phân tử. Các nguyên tố phản ứng ở đây được giữ với nhau do liên kết cộng hóa trị và đó là lý do tại sao các hợp chất này thường được gọi là Hợp chất cộng hóa trị.Liên quan đến hợp chất ion, chúng là chất dẫn điện kém và có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
Thí dụ: Trong Ozone (O3), Oxy kết hợp với việc chia sẻ các electron để tạo thành Ozone.
Hợp chất ion so với hợp chất phân tử
- Các hợp chất ion được hình thành do lực hút tĩnh điện giữa kim loại và phi kim loại, trong khi đó, Hợp chất phân tử được hình thành do sự chia sẻ electron giữa hai phi kim loại.
- Hợp chất phân tử được hình thành khi hai phi kim loại kết hợp hóa học, mặt khác, Hợp chất ion được hình thành giữa kim loại và phi tinh thần.
- Hợp chất phân tử được hình thành do liên kết cộng hóa trị giữa các nguyên tố, trong khi Hợp chất Ionic được hình thành do lực hút tĩnh điện được gọi là liên kết ion.
- Hợp chất phân tử có điểm nóng chảy và nhiệt độ sôi thấp so với Hợp chất ion.
- Hợp chất phân tử có thể ở bất kỳ trạng thái nào, rắn, lỏng hoặc khí ở nhiệt độ phòng, trong khi đó Hợp chất ion luôn ở trạng thái rắn với sự hình thành tinh thể.
- Hợp chất phân tử là chất dẫn điện kém, trong khi Hợp chất ion là chất dẫn điện tốt.